Nach Praxiserfahrungen von Experten besitzt das innovative Taxan nab-Paclitaxel für Patientinnen mit Brustkrebs essenzielle Vorteile wie bessere Verträglichkeit, kurze Infusionsdauer und Verzicht auf Prämedikationen im Vergleich zu konventionellen Taxanen. Taxane zählen beim Brustkrebs zu den aktivsten Zytostatika und sind daher als Basis der systemischen Therapie des metastasierten Mammakarzinoms zu betrachten. Mit dem lösungsmittelfreien nab-Paclitaxel (ABRAXANE®) steht eine moderne Taxan-Formulierung zur Verfügung, mit der in Studien beim metastasierten Brustkrebs gegenüber konventionellen Taxanen eine höhere Ansprechrate mit rascherem Ansprechen und eine verzögerte Progression erreicht wurde.
In den Empfehlungen der Arbeitsgemeinschaft Gynäkologische Onkologie (AGO) werden Anthrazykline und
Taxane mit hohem Evidenz- und Empfehlungsgrad zuoberst in der palliativen Chemotherapie des metastasierten
HER2-negativen/HR-positiven Mammakarzinoms aufgeführt [1]. PD Dr. Cornelia Liedtke (Lübeck) wies darauf
hin, dass die Balance zwischen Effektivität und Toxizität gerade in der palliativen Situation von großer
Bedeutung ist. Daher kommen Anthrazykline wegen ihrer kumulativen Kardiotoxizität oft nicht infrage.
Bei den Taxanen ist Neurotoxizität nicht selten, diese ließe sich allerdings gut handhaben, wenn sie
sich, wie beispielsweise beim nab-Paclitaxel, schnell wieder zurückbilde, betonte Liedtke.
Gute Verträglichkeit, einfache und sichere Applikation
nab-Paclitaxel ist nicht einfach ein anderes Taxan, sondern eine zielgerichtete Chemotherapie
und ein therapeutischer Fortschritt für Frauen mit metastasiertem Brustkrebs, betonte PD Dr. Marc Thill (Frankfurt).
Mittels der nab-Technologie (nanoparticle albumin-bound) ist Paclitaxel an Albumin als
Trägerprotein lipophiler Moleküle gebunden und benötigt daher anders als konventionelle
Taxane keinen Zusatz von Lösungsmitteln, die über ein hohes allergenes Potenzial verfügen.
Eine Standardprämedikation mit Antihistaminika und Dexamethason ist somit bei der nur
30-minütigen Infusion von nab-Paclitaxel nicht erforderlich [2]. Gerade bei den generischen
Taxanen sei nach den Erfahrungen von Prof. Dr. Hans-Joachim Lück (Hannover) häufiger mit
Lösungsmittel-bedingten Toxizitätsproblemen zu rechnen. Insbesondere für gut eingestellte
Diabetiker stelle der Verzicht auf Kortikosteroide einen wichtigen Vorteil dar. Außerdem
verursache wöchentlich appliziertes Kortison Gewichtsprobleme, welche die Lebensqualität
der Patientinnen zusätzlich beeinträchtige, ergänzte Liedtke.
|
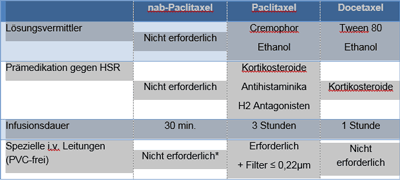
*Die Verwendung eines 15µm Filters wird empfohlen
Tab.: Klinisch praktische Unterschiede zwischen nab-Paclitaxel und anderen Taxanen.
Zudem ermöglicht die patentierte nab-Technologie aufgrund der speziellen Transporteigenschaften von
Albumin eine verstärkte Aufnahme und selektive Anreicherung von Paclitaxel in das Tumorgewebe [3]. Die
dadurch bedingte kürzere Verweildauer von nab-Paclitaxel im Blut führe außerdem zu weniger Neutropenien,
so Thill weiter. Die Wahrscheinlichkeit einer Wirksamkeit von nab-Paclitaxel werde maßgeblich von der
Tumorbiologie bestimmt, welche zum Zeitpunkt der Indikationsstellung besteht, konstatierte Lück. Wie
bei allen Zytostatika stelle eine hohe Proliferationsrate einen brauchbaren Indikator für ein rasches
Therapieansprechen dar. Dies bedeute, dass die Tumorbiologie zum Zeitpunkt der Erst-Diagnose von
nachgeordneter Bedeutung ist, wenn tumorbiologische Faktoren einer Metastase bekannt sind. In den
AGO-Empfehlungen werde deshalb seit Jahren darauf hingewiesen, dass, sofern möglich und der Patientin
zumutbar, eine Biopsie der Metastase gewonnen werden sollte, so Lück.
Verdoppeltes Ansprechen durch tumorgerichtete Wirkung
Die guten Praxiserfahrungen wie hohe Effektivität bei gut handhabbarem Verträglichkeitsprofil
werden durch die Ergebnisse der zulassungsrelevanten Phase-III-Studie bestätigt. Das lösungsmittelfreie
Taxan wurde randomisiert bei 460 vorbehandelten Patientinnen mit meist viszeraler Metastasierung
versus konventionellem Paclitaxel geprüft. Die Gesamtansprechrate als primärer Endpunkt der
Zulassungsstudie wurde durch nab-Paclitaxel nahezu verdoppelt: Auf das konventionelle Taxan
sprachen 19%, auf nab-Paclitaxel 33% der Patientinnen an (p=0,001). Auch in verschiedenen
Subgruppen (Erstlinienbehandlung, Ͱ5Zweitlinienbehandlung, Anthrazyklin-Vorbehandlung,
viszerale Metastasen) erwies sich nab-Paclitaxel konsistent als überlegen. Das primäre
Studienziel wurde also eindeutig erreicht, betonte Liedtke. Hervorzuheben ist das rasche
Ansprechen auf das lösungsmittelfreie Taxan: 91% der Patientinnen hatten bereits im dritten
Zyklus das maximale Ansprechen erreicht; in der Kontrollgruppe gelang dies nur bei 81% [4].
Auch bei mit Anthrazyklin vorbehandelten Patientinnen erwies sich nab-Paclitaxel aufgrund der
signifikanten Verlängerung des Überlebens als sehr effektiv, unabhängig davon, ob das Anthrazyklin
im adjuvanten oder metastasierten Setting eingesetzt worden war (p=0,049 bzw. p=0,022) [5].
Eine hohe Wirksamkeit zeigte nab-Paclitaxel zudem in zwei Phase-II-Studien bei wöchentlicher
Gabe [6-8]. Die anwesenden deutschen Experten schätzen das Regime mit 125 mg/m2 nab-Paclitaxel
wöchentlich über drei Wochen und einer Woche Pause besonders. Dieses Schema mit drei Wochen
on und einer Woche off hat sich wegen seiner hohen Wirksamkeit und des akzeptablen Nebenwirkungsprofils
bewährt, betonte Lück.
Auf Basis der guten Datenlage wird nab-Paclitaxel in den aktuellen Empfehlungen der Organkommission
Mamma der AGO mit dem höchsten Empfehlungsgrad (++) für die palliative Chemotherapie nach
Anthrazyklin-Vorbehandlung des metastasierten HER2-negativen/HR-positiven Mammakarzinoms
aufgeführt [1]. Dabei spielt es keine Rolle, ob Anthrazykline in der metastasierten oder
adjuvanten Situation gegeben wurden. Basierend auf Ihren langjährigen Erfahrungen betrachteten
Liedtke und Lück nab-Paclitaxel als eine hochwirksame Substanz mit einem gut handhabbaren
Nebenwirkungsprofil zur Behandlung des metastasierten Mammakarzinoms. Thills ergänzendes Fazit
lautete dementsprechend: Das Beste zuerst einsetzen.
Literatur: Quelle: Pressegepräch der Celgene GmbH Metastasiertes Mammakarzinom: Für welche Patientin ist nab-Paclitaxel die effektivste Therapie?, Frankfurt, 20. Mai 2015
[1] AGO Guidelines Breast Version 2015.1D
[2] Fachinformation Abraxane® Stand Februar 2015
[3] Desai N. nab technology: a drug delivery platform utilising endothelial gp60 receptor-based
transport and tumour-derived SPARC for targeting. Drug Delivery Report. 2007/2008: 16th Edition, 3741
[4] Gradishar W, et al. 2005. J Clin Oncol 23:7794-7803
[5] Davidson N, et al.2008. EBCC 8, Abstr. 569
[6] Gradishar W, et al.; J Clin Oncol 2009;27;3611-3619
[7] Gradishar W, et al.2012. Clin Breast Cancer 12:313-321
[8] Mirtsching B, et al. 2011. Clin Breast 11:121-128.
| Mai 2015 |
 Inhalt
InhaltVulväre intraepitheliale Neoplasie
Präinvasive genitale Läsionen mit erheblich ange stiegener Inzidenzrate
Literaturreferate
GeparQuattro-Studie:
Neoadjuvante Therapie mit Trastuzu-
Capecitabin zu Anthrazyklin- und Taxan-basierter neoadjuvanter Therapie bei primärem Brustkrebs
Paclitaxel dosisdicht bei fortgeschrittenem Ovarialkrebs
